Нименрикс порошок инструкция по применению

Официальная инструкция
Состав:
После восстановления одна доза (0,5 мл) содержит:
Действующие вещества:
Полисахарид Neisseria meningitidis серогруппы A1 5 мкг.
Полисахарид Neisseria meningitidis серогруппы C 1 мая мкг.
Полисахарид Neisseria meningitidis серогруппы W-135 1 мая мкг.
Полисахарид Neisseria meningitidis серогруппы Y1 5 мкг.
1 конъюгированный с белком-носителем столбнячного анатоксина - 44 мкг.
Вспомогательные вещества: сахароза, трометамол.
Растворитель: натрия хлорид, вода для инъекций.
Производитель:
Местонахождение производителя:
Рейксвег 12 Пуурс, 2870, Бельгия / Rijksweg 12 Puurs, 2870, Belgium.
Фармакотерапевтическая группа:
Фармакологические свойства:
Фармакологические.
механизм действия
Антикапсульни менингококковые антитела защищают от менингококковой заболеваний за счет комплемент-опосредованной бактерицидной активности. По результатам количественного определения с использованием кроличьего комплемента (rSBA) или комплемента человека (hSBA) доказано, что препарат вызывает выработку бактерицидных антител против капсульных полисахаридов Neisseria meningitidis групп A, C, W-135 и Y.
Иммуногенность у младенцев
Было проведено два клинических исследования с участием младенцев:
MenACWY-TT-083 и MenACWY-TT-087. В клиническом исследовании MenACWY-TT-083 первую дозу вводили в возрасте от 6 до 12 недель, вторую дозу - через 2 месяца, а третью (бустерные) дозу - в возрасте примерно 12 месяцев. Вакцину DTaP-HBV-IPV / Hib и 10-валентную пневмококковой вакцины вводили одновременно. Препарат Нименрикс® вызвал выработки бактерицидных антител против четырех менингококковых групп. Ответ против группы C было не слабее ответ, который вызывают лицензированные вакцины MenC-CRM и MenC-TT, учитывая процент с титрами rSBA ≥ 8 через месяц после второй дозы. См. таблицу 1.
Таблица 1. Иммунный ответ (выработку бактерицидных антител) (rSBA *) и (hSBA **) у новорожденных после введения двух доз с интервалом 2 месяца и после введения бустерной дозы в возрасте 12 месяцев (исследования MenACWY-TT-083).
Анализ иммуногенности проводили на первичной когорте «в соответствии с протоколом» (ATP) для анализа иммуногенности.
* Анализ с rSBA проводили в лабораториях Службы общественного здоровья Англии (PHE) в Великобритании.
** Анализ с hSBA проводили в лабораториях компании GSK.
(1) Образцы крови брали через 21-48 дней после вакцинации.
Данные, полученные в исследовании MenACWY-TT-083 поддерживают экстраполяцию данных иммуногенности и режима дозирования для младенцев в возрасте от 12 недель до 6 месяцев. В исследовании MenACWY-TT-087 младенцам применяли или одну первичную дозу в возрасте 6 месяцев с последующей бустерной дозой в возрасте 15-18 месяцев (DTPa-IPV / Hib и 10-валентную пневмококковой конъюгированной вакцины применяли одновременно во время обеих вакцинаций), или три первичных дозы в возрасте 2, 4 и 6 месяцев с бустерной дозой в возрасте 15-18 месяцев. Одна доза, введенная в возрасте 6 месяцев, вызвала стойкие rSBA ответы к серогруппы A, C, W-135 и Y, оценены по проценту субъектов с титрами rSBA ≥ 8 через месяц, которые были сопоставимы с ответами после введения последней дозы из серии трех первичных доз. Бустерная доза вызвала стойкие ответы ко всем четырем менингококковых серогрупп,
Ответы (образование) бактерицидных антител у младенцев в возрасте 6 месяцев определены через месяц после введения одной первичной дозы перед введением бустерной дозы, и через месяц после бустерной дозы, приведенные в таблице 2
Таблица 2. Ответы (образование) бактерицидных антител (rSBA * и hSBA **)) у новорожденных после введения одной дозы в возрасте 6 месяцев и после введения бустерной дозы в возрасте 15-18 месяцев (исследование MenACWY-TT-083).
Анализ иммуногенности проводили на первичной когорте «в соответствии с протоколом» (ATP) для анализа иммуногенности.
* Анализ с rSBA проводили в лабораториях Службы общественного здоровья Англии (PHE) в Великобритании
** Анализ с hSBA проводили в компании Неомед, Лаваль, Канада
(1) отбор крови проводили через месяц после вакцинации
Бактерицидную активность сыворотки крови также измеряли с использованием hSBA в качестве вторичного конечной точки. Хотя и наблюдались сопоставимы ответы к серогруппы A и C при обеих схемах вакцинации, введение одной первичной дозы в возрасте 6 месяцев было связано с более низкими значениями hSBA ответами к серогруппы W-135 и Y, оцененными по проценту субъектов с титрами hSBA ≥ 8 [87.2% (95% ДИ: 74.3, 95.2) и 92.3% (95% ДИ: 81.5, 97.9), согласно] по сравнению с применением трех доз в возрасте 2, 4 и 6 месяцев [100% (95% ДИ: 96.6, 100) и 100% (95% ДИ: 97.1, 100), соответственно] (см. раздел «Особенности применения»). После введения бустерной дозы титры hSBA ко всем четырем серогруппы были сопоставимы в обеих схемах дозирования.
Иммуногенность у детей в возрасте 12-23 месяца
В клинических исследованиях MenACWY-TT-039 и MenACWY-TT-040 одна доза Нименрикс® вызвала ответы rSBA до четырех менингококковых групп, при этом ответ против группы C была сравнима с ответом, который вызывает лицензирована вакцина MenC-CRM, по проценту с титрами rSBA ≥ 8 (таблица 3).
Таблица 3. Ответы (образование) бактерицидных антител (rSBA *) в возрасте 12-23 месяца.
Анализ иммуногенности проводили на когортах ATP для анализа иммуногенности.
(1) Образцы крови брали через 42-56 дней после вакцинации.
(2) Образцы крови брали через 30-42 дней после вакцинации.
* Анализ проводили в лабораториях компании GSK.
В исследовании MenACWY-TT-039 бактерицидную активность сыворотки крови также измеряли с использованием человеческой сыворотки как источника комплемента (hSBA) в качестве вторичного конечной точки (таблица 4).
Таблица 4. Ответы бактерицидных антител (hSBA *) в возрасте 12-23 месяца.
Анализ иммуногенности проводили на когорте ATP для анализа иммуногенности.
(1) Образцы крови брали через 42-56 дней после вакцинации.
* Анализ проводили в лабораториях компании GSK.
В исследовании Men ACWY-TT-104 иммунный ответ после одной или двух доз препарата Нименрикс® с интервалом 2 месяца оценивали через месяц после вакцинации. Препарат Нименрикс® вызвал бактерицидные ответы против всех четырех групп, аналогичные по проценту с титром rSBA ≥ 8 и значение GMT после одной или двух доз (таблица 5).
Таблица 5. Ответы бактерицидных антител (rSBA) * в возрасте 12-14 месяцев.
Анализ иммуногенности проводили на когорте «в соответствии с протоколом» (ATP) для анализа иммуногенности.
(1) Образцы крови брали через 21-48 дней после вакцинации.
* Анализ проводили в лабораториях Службы общественного здоровья Англии (PHE).
В исследовании MenACWY-TT-104 бактерицидную активность сыворотки крови также измеряли с использованием hSBA в качестве вторичного конечной точки. Препарат Нименрикс® вызвал бактерицидные ответы против групп W-135 и Y, которые в случае введения двух доз были выше процентами с титром hSBA ≥ 8 по сравнению с одной дозой. Аналогичные ответы по процентам с титром hSBA ≥ 8 наблюдались против групп A и C (таблица 6).
Таблица 6. Ответы бактерицидных антител (hSBA) * у детей в возрасте 12-14 месяцев.
Анализ иммуногенности проводили на когорте «в соответствии с протоколом» (ATP) для анализа иммуногенности.
(1) Образцы крови брали через 21-48 дней после вакцинации.
* Анализ проводили в лабораториях компании GSK.
Устойчивость иммунного ответа оценивали по rSBA и hSBA течение периода до 5 лет у детей, прошедших начальную вакцинацию в рамках исследования MenACWY-TT-027 (таблица 7).
Tаблиця 7. Данные об устойчивости за 5 лет у детей в возрасте 12-23 месяца при вакцинации (исследование MenACWY-TT-032, расширение исследования 027).
Устойчивость иммуногенности анализировали с использованием когорты ATP на 5 году. Ошибка отбора, связана главным образом с повторной вакцинацией субъектов с титрами rSBA <8 группы C и исключением таких субъектов из следующих моментов времени, могла привести к завышенной оценке титров.
* Анализ с rSBA проводили в лабораториях PHE в Великобритании.
** Анализ проводили в лабораториях компании GSK.
Иммуногенность у детей 2-10 лет
В исследовании MenACWY-TT-081 было продемонстрировано, что препарат Нименрикс® не менее эффективным, чем другая лицензирована вакцина MenC-CRM, с точки зрения ответа на группу C [94,8% (95% ДИ: 91,4; 97, 1) и 95,7% (95% ДИ: 89,2; 98,8), согласно]. Значение GMT было ниже для группы препарата Нименрикс® [2795 (95% ДИ: 2393; 3263)] по сравнению с вакциной MenC-CRM [5292 (95% ДИ: 3815; 7340)].
В исследовании MenACWY-TT-038 вакцина Нименрикс® оказалась не менее эффективной по сравнению с лицензированной вакциной ACWY-PS с точки зрения реакции на четыре группы (A, C, W-135 и Y) (см. Таблицу 8).
Таблица 8. Ответы бактерицидных антител (rSBA *) на Нименрикс® и вакцину ACWY-PS в возрасте 2-10 лет через 1 месяц после вакцинации (исследование MenACWY-TT-038).
Анализ иммуногенности проводили на когорте ATP для анализа иммуногенности.
VR - ответ на вакцину, определенная как доля субъектов со следующими показателями:
• титры rSBA ≥ 32 для изначально серонегативных субъектов (то есть титр rSBA к вакцинации <8);
• не менее 4-кратный рост титров rSBA после вакцинации по сравнению с титрами перед вакцинацией в первоначально серопозитивных субъектов (то есть титр rSBA к вакцинации ≥ 8).
* Анализ проводили в лабораториях компании GSK.
Устойчивость иммунного ответа оценивали у детей, прошедших начальную вакцинацию в рамках исследования MenACWY-TT-081 (таблица 9).
Таблица 9. Данные по устойчивости за 44 месяца в возрасте 2-10 лет при вакцинации (исследование MenACWY-TT-088, расширение исследования 081).
Анализ иммуногенности проводили на когорте ATP для анализа устойчивости, адаптированной для каждого момента времени.
* Анализ с rSBA проводили в лабораториях PHE в Великобритании.
** Анализ проводили в лабораториях компании GSK.
Устойчивость иммунного ответа оценивали по hSBA через 1 год после вакцинации у детей 6- 10 лет, прошедших начальную вакцинацию в рамках исследования MenACWY-TT-027 (таблица 10) (см. Раздел «Особенности применения»).
Таблица 10. Данные по устойчивости через 1 месяц после вакцинации и через 1 год (hSBA *) в возрасте 6-10 лет.
Анализ иммуногенности проводили на когорте ATP для анализа устойчивости.
* Анализ проводили в лабораториях компании GSK.
Иммуногенность у подростков в возрасте 11-17 лет и взрослых в возрасте ≥ 18 лет
В двух клинических исследованиях, которые проводились с участием подростков в возрасте 11-17 лет (исследование MenACWYTT-036) и взрослых в возрасте 18-55 лет (исследование MenACWYTT-035), субъектам вводили или одну дозу Нименрикс®, или одну дозу вакцины ACWY-PS.
Было продемонстрировано, что препарат Нименрикс® иммунологически не менее эффективным, чем вакцина ACWY-PS, с точки зрения ответа на вакцину (таблица 11).
Анализ иммуногенности проводили на когортах ATP для анализа иммуногенности.
VR - ответ на вакцину.
* Анализ проводили в лабораториях компании GSK.
Устойчивость иммунного ответа оценивали в течение периода до 5 лет после вакцинации у подростков, прошедших вакцинацию в рамках исследования MenACWY-TT-036 (таблица 12).
Таблица 12. Данные об устойчивости за 5 лет (rSBA *) у подростков в возрасте 11-17 лет при вакцинации.
Анализ иммуногенности проводили на когорте ATP для анализа устойчивости, адаптированной для каждого момента времени.
* Анализ с rSBA проводили в лабораториях PHE в Великобритании.
Устойчивость иммунного ответа оценивали по hSBA течение периода до 5 лет после вакцинации у подростков и взрослых, которые прошли начальную вакцинацию в рамках исследования MenACWYTT-052 (таблица 13) (см. Раздел «Особенности применения»).
Таблица 13. Данные об устойчивости за 1 месяц после вакцинации (исследование MenACWY-TT-052) и за 5 лет (исследование MenACWY-TT-059) (hSBA *) у подростков и взрослых в возрасте 11-25 лет.
Анализ иммуногенности проводили на когорте ATP для анализа устойчивости, адаптированной для каждого момента времени.
* Анализ проводили в лабораториях компании GSK.
В отдельном исследовании (MenACWY-TT-085) одну дозу Нименрикс® вводили 194 взрослым ливанцам в возрасте от 56 лет (включая 133 человека в возрасте 56-65 лет и 61 человек в возрасте> 65 лет). Процент субъектов с титрами rSBA (по результатам измерения в лабораториях компании GSK) ≥ 128 перед вакцинацией варьировался от 45% (группа C) до 62% (группа Y). В целом через месяц после вакцинации процент вакцинированных с титрами rSBA ≥ 128 варьировался от 93% (группа C) до 97% (группа Y). В подгруппе лиц в возрасте> 65 лет процент вакцинированных с титрами rSBA ≥ 128 через месяц после вакцинации варьировался от 90% (группа A) до 97% (группа Y).
Ответ на Бустерные дозу субъектов, которые ранее прошли вакцинацию конъюгированной менингококковой вакциной против бактерий Neisseria meningitidis
Вакцинация Бустерная дозой препарата Нименрикс® у субъектов, которые ранее прошли вакцинацию одновалентной (MenC-CRM) или четырехвалентного конъюгированной менингококковой вакциной (MenACWY-TT), исследовали у субъектов в возрасте от 12 месяцев, получили Бустерная дозу вакцины. Наблюдались устойчивые анамнестические ответа на антигены в введенной вакцине.
Ответ на препарат Нименрикс® у субъектов, которые ранее прошли вакцинацию простой полисахаридной вакциной против бактерий Neisseria meningitidis
В исследовании MenACWY-TT-021, которое проводилось на субъектах возрасте 4,5-34 лет, иммуногенность препарата Нименрикс®, который вводили в интервале между 30 и 42 месяцами после вакцинации вакциной ACWY-PS, сравнивали с иммуногенностью препарата Нименрикс®, который вводили субъектам в соответствующей возрастной группе, не проходили вакцинацию одной менингококковой вакциной в течение последних 10 лет. Иммунный ответ (титр rSBA ≥ 8) против всех групп (A, C, W-135 и Y) наблюдалась во всех субъектах независимо от анамнеза вакцинации менингококковой вакцинами. Значение GMT rSBA были значительно ниже у субъектов, 12 получивших дозу вакцины ACWY-PS за 30-42 месяца к препарату Нименрикс®, однако 100% субъектов достигли титров rSBA ≥ 8 для всех менингококковых групп (A, C, W -135 и Y) (см. раздел «Особенности применения»).
Дети (от 2 до 17 лет) с анатомической или функциональной аспленией
В исследовании MenACWY-TT-084 сравнивали иммунный ответ на введение двух доз препарата Нименрикс® с интервалом в 2 месяца среди 43 субъектов возрасте 2-17 лет с анатомической или функциональной аспленией и 43 субъектов соответствующего возраста с нормальной функцией селезенки. Через месяц после введения первой дозы и через месяц после введения второй одинаковый процент субъектов в двух группах имели титры rSBA ≥1: 8 и ≥1: 128 и hSBA титры ≥1: 4 и ≥1: 8.
Фармакокинетика.
Оценка фармакокинетических свойств вакцин не является обязательной.
Показания к применению:
Вакцина Нименрикс® показана для активной иммунизации лиц в возрасте от 6 недель против инвазионных менингококковых заболеваний, вызванных Neisseria meningitidis серогруппы A, C, W-135 и Y.
Противопоказания:
Гиперчувствительность к действующим веществам или любых вспомогательных веществ, входящих в состав вакцины (см. Раздел «Состав»).
Особенности применения:
Нименрикс® при каких обстоятельствах нельзя вводить внутрисосудисто, внутрикожно или подкожно.
Согласно должным клинической практике, перед вакцинацией следует оценить анамнез (особенно на предмет предыдущей вакцинации и возможного возникновения побочных реакций) и провести клинический осмотр.
Необходимо обеспечить возможность предоставления надлежащей медицинской помощи и медицинского наблюдения при возникновении анафилактических реакций, которые в редких случаях могут развиться после введения вакцины.
интеркуррентные заболевания
Применение вакцины Нименрикс® должно быть отложено у лиц, страдающих от острых заболеваний, сопровождающихся повышенной температурой. Однако, наличие легких незначительных проявлений инфекционных заболеваний, таких как простуда, не является основанием для отложения вакцинации.
Обморок
Синкопе (обморок) может во время или даже перед проведением вакцинации, особенно у подростков, как психогенная реакция на инъекцию иглой. Это может сопровождаться определенными неврологическими симптомами, такими как временное нарушение зрения, парестезии и тонико-клонические движения конечностей во время выхода из этого состояния. Важно обеспечить условия для избежания травмирования вследствие потери сознания.
Тромбоцитопения и нарушение свертывания крови
Нименрикс® следует применять с осторожностью у пациентов с тромбоцитопенией или любым нарушением свертывания крови, поскольку при введении у таких пациентов может возникнуть кровотечение.
иммунодефицит
Может ожидаться, что у пациентов, получающих иммуносупрессивное лечение, или у пациентов с иммунодефицитом может не возникнуть надлежащая иммунная реакция.
Лица с наследственными дефицитами системы комплемента (например дефицитами C5 или C3 компонентов) и лица, которым применяют препараты, ингибирующие терминальную активацию комплемента (например екулизумаб) имеют повышенный риск инвазивного менингококкового заболевания вызванного Neisseria meningitidis серогруппы A, C, W-135 и Y, даже при условии образования антител после вакцинации препаратом Нименрикс®.
Защита от менингококкового заболевания
Нименрикс® обеспечивает защиту только от Neisseria meningitidis серогруппы A, C, W-135 и Y. Вакцина не обеспечивает защиту от других серогрупп Neisseria meningitidis . Защитная иммунный ответ может развиваться не у всех провакцинированных человек.
Влияние предварительной вакцинации простой полисахаридной менингококковой вакциной
В субъектов, проходили предварительную вакцинацию простой полисахаридной менингококковой вакциной и в течение 30-42 месяцев после этого прошли вакцинацию препаратом Нименрикс®, наблюдались более низкие средние геометрические значения титров (GMT) по результатам бактерицидного анализа сыворотки крови с использованием кроличьего комплемента (rSBA), чем у субъектов, не проходили вакцинацию одной менингококковой вакциной в течение последних 10 лет (см. раздел «Фармакологические»). Клиническая значимость результатов этого наблюдения неизвестна.
Влияние предварительной вакцинации антитела к столбнячного анатоксина
Безопасность и иммуногенность препарата Нименрикс® оценивались в условиях последовательного или одновременного введения с вакциной, содержащей дифтерийный и столбнячный анатоксины, ацелюлярных коклюш, инактивированные полиовирусы (1, 2 и 3), поверхностный антиген вируса гепатита B и полирибозилрибозофосфат Haemophilus influenzae типа b, кон ' югований с столбнячным анатоксином (DTaP-HBV-IPV / Hib), на втором году жизни. В случае введения препарата Нименрикс® через месяц после вакцины DTaP-HBV-IPV / Hib значение GMT rSBA против серогруппы A, C и W-135 были ниже по сравнению с одновременным введением вакцин (см. Раздел «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий »). Клиническая значимость результатов этого наблюдения неизвестна.
Иммунный ответ у младенцев в возрасте от 6 до 12 месяцев
Применение одной дозы в возрасте 6 месяцев было связано с более низкими значениями титров на серогруппы W-135 и Y по результатам бактерицидного анализа сыворотки крови с использованием комплемента человека (hSBA) по сравнению с применением трех доз в возрасте 2, 4 и 6 месяцев (см. раздел «Фармакологические»). Клиническая значимость этих результатов неизвестна. Если для младенца в возрасте от 6 до 12 месяцев ожидается определенный риск инвазивного менингококкового заболевания с участием серогруппы W-135 и Y, можно рассмотреть целесообразность введения второй первичной дозы Нименрикс® через 2 месяца.
Иммунные ответы у детей 12-14 месяцев
Дети 12-14 месяцев имели аналогичные ответы rSBA на серогруппы A, C, W-135 и Y через месяц после одной дозы препарата Нименрикс® или через месяц после двух доз препарата Нименрикс® с интервалом два месяца.
Применение одной дозы было связано с более низкими значениями титров на серогруппы W-135 и Y по результатам hSBA по сравнению с применением двух доз с интервалом два месяца. Аналогичные ответы на группы A и C наблюдались после одной или двух доз (см. Раздел «Фармакологические»). Клиническая значимость этих результатов неизвестна. Если для ребенка ожидается определенный риск инвазивного менингококкового заболевания с участием серогруппы W135 и Y, можно рассмотреть целесообразность введения второй дозы Нименрикс® через 2 месяца. Информацию о снижении уровня антител к группе A или группы C после первой дозы препарата Нименрикс® в возрасте 12-23 месяца см. в подразделе «Устойчивость титров бактерицидных антител в сыворотке крови».
Устойчивость титров бактерицидных антител в сыворотке крови
При проведении анализа hSBA после введения препарата наблюдали снижение титров бактерицидных антител в сыворотке крови к серогруппы A (см. Раздел «Фармакологические»). Клиническая значимость снижения титров антител hSBA к группе A неизвестна. Однако, если для лица ожидается определенный риск инфицирования серогруппы A, и если человек получил дозу Нименрикс® более около года назад, можно рассмотреть целесообразность введения бустерной дозы.
Для серогруппы A, C, W-135 и Y наблюдалось снижение титров антител со временем. Клиническая значимость снижения титров антител неизвестна. Целесообразность бустерной дозы можно рассмотреть для лиц, прошедших вакцинацию в раннем детском возрасте, и для которых остался высокий риск развития менингококкового заболевания, вызванного серогруппы A, C, W-135 или Y (см. Раздел «Фармакологические»).
Влияние Нименрикс® на концентрации противостолбнячная антител
Хотя после вакцинации препаратом Нименрикс® наблюдалось повышение концентрации антител к столбнячного анатоксина (TT), препарат Нименрикс® не заменяет иммунизацию против столбняка.
Введение препарата Нименрикс® одновременно или за месяц до вакцины, содержащей столбнячный анатоксин, на втором году жизни не ухудшает ответ на столбнячный анатоксин и не оказывает значительного влияния на безопасность. Данные для лиц другого возраста отсутствуют.
Это лекарственное средство содержит менее 1 ммоль (23 мг) / дозу натрия, то есть практически свободный от натрия.
Применение в период беременности или кормления грудью:
беременность
Доступные ограниченные данные по применению вакцины Нименрикс® беременным женщинам. Исследования вакцины Нименрикс® на животных не свидетельствуют о прямой или косвенный вредное влияние на беременность, эмбриофетальной развитие, роды или постнатальное развитие.
Нименрикс® следует применять в период беременности только при наличии четкой потребности и если ожидаемая польза превышает потенциальные риски для плода.
кормление грудью
Неизвестно, выводится вакцина Нименрикс® в грудное молоко. Нименрикс® следует применять у женщин, кормящих грудью, только если ожидаемая польза превышает потенциальные риски.
фертильность
Исследования на животных не свидетельствуют о прямой или косвенный вредное воздействие на фертильность.
Способность влиять на скорость реакции при управлении автотранспортом:
Исследование влияния вакцины Нименрикс® на способность управлять автотранспортом или другими механизмами не проводились. Однако некоторые побочные реакции (указанные в разделе «Побочные реакции») могут повлиять на способность управлять автотранспортом или другими механизмами.
Дети:
Применяют детям в возрасте от 6 недель.
Способ применения и дозы:
первичная иммунизация
Младенцам в возрасте от 6 недель до 6 месяцев: нужно вводить две дозы по 0,5 мл с интервалом в 2 месяца.
Детям в возрасте от 6 месяцев и взрослым: следует вводить одну дозу 0,5 мл.
Некоторым лицам может быть целесообразным введение дополнительной начальной дозы препарата Нименрикс® (см. Раздел «Особенности применения»).
бустерные дозы
После завершения курса первичной иммунизации младенцам в возрасте от 6 недель до 12 месяцев, Бустерная дозу следует вводить в возрасте 12 месяцев с соблюдением интервала в 2 месяца после последней вакцинации препаратом Нименрикс® (см. Раздел «Фармакологические»).
Лицам в возрасте от 12 месяцев, которые уже прошли первичную вакцинацию конъюгированной или простой полисахаридной менингококковой вакциной, препарат Нименрикс® можно вводить в качестве бустерной дозы (см. Разделы «Особенности применения» и «Фармакологические»).
способ применения
Иммунизацию следует выполнять только путем инъекции.
У новорожденных заказным местом инъекции является переднелатеральную участок бедра. У лиц старше 1 года заказным местом инъекции является переднелатеральную участок бедра или дельтовидную мышцу (см. Разделы «Особенности применения» и «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий»).
При проведении иммунизации на территории Украины следует руководствоваться действующими приказами МЗ Украины для проведения профилактических прививок.
Инструкция по использованию вакцины:
Инструкции по восстановлению вакцины с помощью растворителя, поставляемого в ампулах
Нименрикс® следует восстановить путем добавления всего содержимого ампулы с растворителем во флакон, содержащий порошок. Для этого отломите верхушку ампулы, наберите растворитель в шприц и добавьте растворитель до порошка. Смесь следует хорошо взбалтывать до тех пор, пока порошок полностью не растворится в растворителе.
Инструкции по восстановлению вакцины с помощью растворителя, поставляемого в предварительно наполненных шприцах
Нименрикс® восстанавливают путем добавления всего содержимого предварительно заполненного шприца во флакон, содержащий порошок.
Для подключения иглу к шприцу см. рисунок ниже. Следует отметить, что шприц, который поставляется с вакциной Нименрикс®, может несколько отличаться от шприца, изображенного на рисунке (не иметь резьбы). В таком случае иглу следует прикрепить без закручивания.
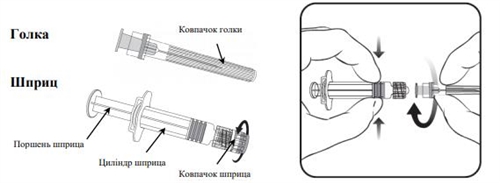
- Держите цилиндр шприца одной рукой (не следует держать шприц с поршень), открутите колпачок шприца, вращая его против часовой стрелки.
- Для подключения иглу к шприцу, поворачивайте иглу по часовой стрелке до тех пор, пока не почувствуете, что игла зафиксирована (см. Рисунок).
- Снимите колпачок иглы для этого может потребоваться незначительное усилие.
- Добавьте растворитель до порошка. После добавления растворителя к порошка смесь следует хорошо встряхивать до тех пор, пока порошок полностью не растворится в растворителе.
после разведения
Восстановлена вакцина представляет собой прозрачный бесцветный раствор.
Перед введением восстановленную вакцину следует визуально осмотреть на наличие каких-либо посторонних примесей и / или изменение физических свойств. В случае появления таких отклонений вакцину следует утилизировать.
После восстановления вакцину следует сразу использовать.
Хотя и не рекомендуется задерживаться с введением вакцины, стабильность вакцины сохраняется в течение 8:00 при температуре 30 ° С после разведения.
Если вакцина не была использована в течение 8:00, вакцину вводить нельзя.
Для введения вакцины используют новую иглу.
Любой неиспользованный препарат или отходы следует утилизировать в соответствии с местными требованиями.
Передозировка:
Случаи передозировки неизвестны.
Побочные действия:
профиль безопасности
Приведенная ниже информация по безопасности препарата Нименрикс® основана на данных из следующих клинических исследований:
- Обобщенный анализ данных полученных от 9621 субъекта, которым применяли одну дозу Нименрикс®. Среди них было 3079 детей в возрасте от 12 до 23 месяцев, 909 детей в возрасте от 2 до 5 лет, 990 детей в возрасте от 6 до 10 лет, 2317 подростков (от 11 до 17 лет) и 2326 взрослых (от 18 до 55 лет).
- Данные по исследованию с участием младенцев в возрасте от 6 до 12 недель на время введения первой дозы (исследование MenACWY-TT-083), 1052 субъекты получили хотя бы одну дозу в рамках начальной серии из 2 или 3 доз препарата Нименрикс®, и 1008 суб объектов получили Бустерная дозу в возрасте примерно 12 месяцев.
Данные по безопасности были также оценены в отдельном исследовании, в котором одну дозу Нименрикс® вводили 274 лицам в возрасте от 56 лет.
Местные и общие побочные реакции
В группах субъектов 6-12 недель и 12-14 месяцев, которые получили 2 дозы Нименрикс®, с интервалом 2 месяца, введение первой и второй доз было связано с аналогичным местной и системной реактогенностью.
Профиль местных и общих побочных реакций бустерной дозы Нименрикс® у субъектов в возрасте от 12 месяцев до 30 лет, после первичной вакцинации препаратом Нименрикс®, или другими конъюгированными или простыми полисахаридными менингококковой вакцинами был аналогичным профиля местных и общих побочных реакций, который наблюдался после первичной вакцинации препаратом Нименрикс®, исключая симптомов желудочно-кишечного тракта (включая диарею, рвоту и тошноту), которые возникали очень часто среди субъектов в возрасте от 6 лет.
Перечень побочных реакций в виде таблицы
Зарегистрированные побочные реакции указано по приведенным ниже категориям в зависимости от частоты.
Очень часто: (≥ 1/10)
Частые: (от ≥ 1/100 до <1/10)
Нечасто (от ≥ 1/1000 до <1/100)
Редкие: (от ≥ 1/10 000 до <1/1000)
Редкие (<1/10 000)
Частота неизвестна: частоту невозможно установить, исходя из имеющихся данных.
В таблице 14 приведены побочные реакции, зарегистрированные в ходе исследований на субъектах в возрасте от 6 недель до 55 лет и во время пострегистрационных применения препарата. Побочные реакции, зарегистрированные у субъектов в возрасте> 55 лет, были аналогичные реакциям, которые наблюдались у взрослых младшего возраста.
Таблица 14. Сводная таблица побочных реакций с системно-органным классом.
| Класс систем органов | Частота | побочные реакции |
| Нарушение метаболизма и питания | очень часто | снижение аппетита |
| Со стороны психики | очень часто | раздражительность |
| редкие | бессонница Плач | |
| Со стороны нервной системы | очень часто | сонливость Головная боль |
| редкие | гипестезия головокружение | |
| Со стороны желудочно-кишечного тракта | частые | диарея рвота тошнота * |
| Со стороны кожи и подкожной ткани | редкие | зуд высыпания ** |
| Со стороны опорно-двигательного аппарата и соединительной ткани | редкие | миалгия Боль в конечностях |
| Общие нарушения и реакции в месте введения | очень часто | повышение температуры Отеки в месте инъекции Боль в месте инъекции Покраснение в месте инъекции утомляемость |
| частые | Гематома в месте инъекции * | |
| редкие | плохое самочувствие Уплотнения в месте инъекции Зуд в месте инъекции Жар в месте инъекции Потеря чувствительности в месте инъекции | |
| Частота неизвестна *** | Значительная отечность конечностей в месте инъекции, часто связана с эритемой, иногда охватывает соседние суставы, или отечность всей конечности, в которую было выполнено инъекцию |
Тошнота и гематома в месте инъекции возникали у младенцев с частотой «Нечасто».
** Высыпания возникало у младенцев с частотой «Часто».
*** побочная реакция, обнаруженная в пост-маркетинговых исследованиях.
Отчет о побочных реакциях.
Отчет о побочных реакциях после регистрации лекарственного средства имеет важное значение. Это позволяет проводить непрерывный мониторинг соотношения между пользой и рисками, связанными с применением этого препарата. Врачам следует отчитываться о любых подозреваемые побочные реакции в соответствии с требованиями законодательства.
несовместимость
Учитывая отсутствие исследований совместимости, это лекарственное средство не следует смешивать с другими лекарственными средствами.
Лекарственное взаимодействие:
Младенцам препарат Нименрикс® можно применять одновременно с комбинированными вакцинами DTaP-HBV-IPV / Hib и 10-валентной пневмококковой конъюгированной вакциной.
Детям от одного года и взрослым Нименрикс® можно применять попутно с такими вакцинами: вакцины для профилактики гепатита A (HAV) и гепатита B (HBV), вакцина для профилактики кори, паротита и краснухи (MMR), вакцина для профилактики кори, паротита, краснухи и ветряной оспы (MMRV), 10-валентной пневмококковой конъюгированной вакцины или неадьювантнои вакцины для сезонной профилактики гриппа.
На втором году жизни препарат Нименрикс® можно применять одновременно с комбинированными вакцинами против дифтерии / столбняка / ацелюлярная коклюша (DTaP), включая комбинации вакцин DTaP с вакцинами против гепатита B, инактивированного полиовируса или гемофильной палочки Haemophilus influenzae типа b (HBV, IPV или Hib ), такой как вакцина DTaP-HBV-IPV / Hib, и 13-валентной пневмококковой конъюгированной вакциной.
Лицам в возрасте от 9 до 25 лет, вакцину Нименрикс® можно применять одновременно с Бивалентный (тип 16 и 18) рекомбинантной вакциной против вируса папилломы человека (HPV2).
По возможности вакцину Нименрикс® и вакцину, содержащую столбнячный анатоксин (TT), например, вакцину DTaP-HBV-IPV / Hib, следует вводить попутно, или провести вакцинацию препаратом Нименрикс® минимум за месяц до применения вакцины, содержащей TT.
Через месяц после одновременного применения 10-валентной пневмококковой конъюгированной вакцины отмечалось уменьшение средней геометрической концентрации антител (GMCs) и GMT антител по результатам анализа опсонофагоцитуючои активности (OPA) для одного пневмококкового серотипа (18C, конъюгированный с белком-носителем столбнячного анатоксина) . Клиническая значимость этого наблюдения неизвестна. Не отмечалось никакого влияния сопутствующего введения на иммунный ответ к другим девяти пневмококковых серотипов.
Через месяц после одновременного применения с комбинированной вакциной для профилактики дифтерии, столбняка, коклюша (ацелюлярных компонент) (адсорбированная, с уменьшенным содержанием антигенов) (Tdap) субъектам в возрасте от 9 до 25 лет, низкие значения GMCs наблюдались ко всем антигенам коклюша (коклюшный анатоксин [PT], филаментных гемагглютинин [FHA] и пертактин [PRN]). Более 98% субъектов имели концентрации антител против PT, FHA или PRN выше предельной границы определения. Клиническая значимость данного наблюдения неизвестно. Одновременное применение не оказало влияния на иммунные ответы к Нименриксу или к антигенам столбняка или дифтерии, входящих в состав Tdap.
Если вакцину Нименрикс® необходимо применять одновременно с другими вакцинами для инъекций, вакцины следует всегда вводить в разные места для инъекций.
У пациентов, получающих иммуносупрессивное лечение, может не возникнуть надлежащая иммунный ответ.
Срок годности:
Вакцина - 4 года.
Растворитель - 5 лет.
после восстановления
После восстановления вакцину следует сразу использовать. Хотя и не рекомендуется задерживаться с введением вакцины, стабильность вакцины сохраняется в течение 8:00 при температуре 30 ° С после разведения. Если вакцина не была использована в течение 8:00, вакцину вводить нельзя.
Условия хранения:
Хранить при температуре от 2 до 8 ° С. Защищать от света. Хранить в недоступном для детей месте. Не замораживать.
После восстановления вакцину следует сразу использовать. Если вакцина не была использована сразу, условия хранения восстановленной вакцины см. в разделе «Срок годности».
Растворитель можно хранить при комнатной температуре (25 ° С).
Если вакцина или растворитель были заморожены, их следует утилизировать.
Форма выпуска / упаковка:
По 1 флакону с порошком (1 доза) в комплекте с растворителем (0,5 мл) в предварительно наполненном шприце и двумя иглами упаковывают в блистер и вкладывают в картонную коробку вместе с инструкцией по применению.
По 1 флакону с порошком (1 доза) в комплекте с растворителем (0,5 мл) в предварительно наполненном шприце без иглы упаковывают в блистер; 10 блистеров вкладывают в картонную коробку вместе с инструкцией по применению.
Категория отпуска:
По рецепту.
Дополнительно:
міжнародна непатентована назва: Meningococcal polysaccharide serogroups A, C, W-135 and Y conjugate vaccineосновні властивості лікарської форми: Німенрикс™ – це неадсорбована ліофілізована вакцина, яка поставляється в комплекті з розчинником. Порошок білого кольору. Розчинник прозорий та безбарвний. Готова відновлена вакцина не містить консервантів.Вакцина складається з очищених капсульних полісахаридів Neisseria meningitidis серогруп A, C, W та Y, кожен з яких кон’югований з правцевим анатоксином у відповідних співвідношеннях.Німенрикс™ відповідає вимогам Всесвітньої Організації Охорони Здоров’я до полісахаридних кон’югованих вакцин для профілактики менінгококової інфекції.
Форма випускуЛіофілізат для розчину для ін’єкцій.
НесумісністьВраховуючи відсутності досліджень сумісності, цей лікарський засіб не слід змішувати з іншими лікарськими засобами.
Представництво в УкраїніТОВ Пфайзер Україна, 03680, м. Київ, вул. Амосова 12, тел.: (044) 391 60 50, факс: (044) 391 60 51.
Дополнительные данные
| Тип данных | Сведения из реестра |
|---|---|
| Торговое наименование: | Нименрикс порошок |
| Производитель: | Пфайзер Менюфекчуринг Бельгия НП / Pfizer Manufacturing Belgium NV |
| Форма выпуска: | По 1 флакону с порошком (1 доза) в комплекте с растворителем (0,5 мл) в предварительно наполненном шприце и двумя иглами упаковывают в блистер и вкладывают в картонную коробку вместе с инструкцией по применению. По 1 флакону с порошком (1 доза) в комплекте с растворителем (0,5 мл) в предварительно наполненном шприце без иглы упаковывают в блистер; 10 блистеров вкладывают в картонную коробку вместе с инструкцией по применению. |
| Регистрационное удостоверение: | UA/16901/01/01 от 15.08.2018 |
| МНН: | Meningococcus A,C,Y,W-135, tetravalent purified polysaccharides antigen conjugated |
| Условия отпуска: | По рецепту. |
| Состав: | После восстановления одна доза (0,5 мл) содержит: Действующие вещества: Полисахарид Neisseria meningitidis серогруппы A1 5 мкг. Полисахарид Neisseria meningitidis серогруппы C 1 мая мкг. Полисахарид Neisseria meningitidis серогруппы W-135 1 мая мкг. Полисахарид Neisseria meningitidis серогруппы Y1 5 мкг. 1 конъюгированный с белком-носителем столбнячного анатоксина - 44 мкг. Вспомогательные вещества: сахароза, трометамол. Растворитель: натрия хлорид, вода для инъекций. |
| Фармакологическая группа: | Антибактериальные вакцины. Вакцина для профилактики менингококковой инфекции |
| Код АТХ: | J07AH08 - Менингококковый a, c, y, w-135, тетравалентний очищенный полисах. антиген конъюгированный |
| Заявитель: | Пфайзер ЕЙЧ.СИ.ПИ. КОРПОРЕЙШН |
| Адрес заявителя: | 235 Ист 42-я стрит, Нью-Йорк, НЙ 10017-5755, США |